A Tabela Periódica não é apenas um quadro cheio de símbolos e números: ela é um dos pilares da Química e da compreensão da matéria. Seja no laboratório, na indústria ou em uma questão do ENEM, entender sua lógica facilita a vida de qualquer estudante.
Isso porque a organização dos elementos não foi feita ao acaso ela carrega uma história rica, regras precisas e muita ciência. E se você acha tudo isso complicado, respire fundo: este artigo do Fala Ciência vai te mostrar a Tabela Periódica de forma clara, prática e atualizada com as últimas descobertas.
Tabela Periódica Completa e Atualizada: importância para a Química
A Tabela Periódica é um modelo que agrupa todos os elementos químicos conhecidos e suas propriedades. Eles estão organizados em ordem crescente de número atômico, ou seja, o número de prótons no núcleo de cada átomo. Dessa maneira, é possível prever comportamentos, reações e relações entre os elementos.
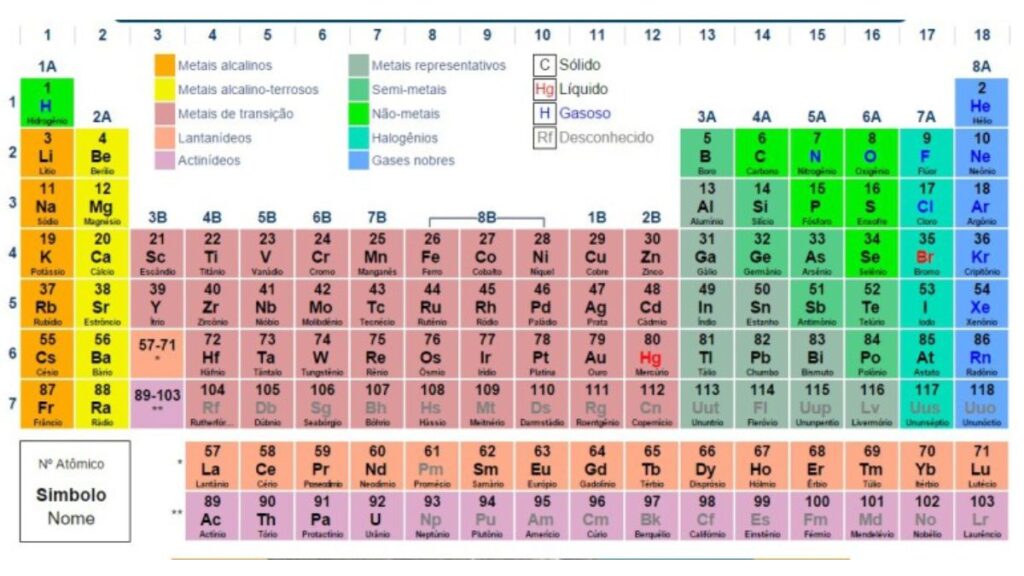
No total, a versão mais recente da Tabela reúne 118 elementos químicos, dos quais 92 são naturais e 26 são artificiais. Cada quadrado da tabela representa um elemento, contendo seu nome, símbolo e número atômico. Com isso, ela se torna uma verdadeira bússola para quem deseja entender a estrutura da matéria.
Desvendando os períodos: o que significam as linhas horizontais?
Os períodos são as linhas horizontais da Tabela e totalizam sete no modelo atual. Eles indicam a quantidade de camadas eletrônicas que um átomo possui.
- 1º Período: 2 elementos
- 2º Período: 8 elementos
- 3º Período: 8 elementos
- 4º e 5º Períodos: 18 elementos cada
- 6º e 7º Períodos: 32 elementos cada
Sendo assim, para evitar que a tabela fique visualmente desproporcional, a série dos lantanídeos e a série dos actinídeos costuma ser representada separadamente, abaixo do corpo principal.
Veja também:
- Mudanças climáticas: causas e consequências para o planeta
- Recursos naturais renováveis e não renováveis: o que são, tipos e importância
- Atividades de português 4º ano de interpretação de texto e gramática
Colunas verticais que revelam segredos: os grupos ou famílias
Os grupos — também chamados de famílias — são as colunas verticais que agrupam elementos com o mesmo número de elétrons na camada de valência. Ao todo, são 18 grupos, e muitos compartilham propriedades químicas similares.
Veja alguns destaques:
- Grupo 1 (1A): Metais Alcalinos — lítio, sódio, potássio, entre outros.
- Grupo 2 (2A): Metais Alcalinoterrosos — como cálcio e magnésio.
- Grupo 17 (7A): Halogênios — flúor, cloro, bromo, iodo, astato e tenessino.
- Grupo 18 (8A): Gases Nobres — como hélio, neônio, argônio e oganessônio.
Além disso, os metais de transição ocupam a parte central da Tabela e incluem elementos como ferro, cobre, ouro e platina.
A evolução histórica da tabela: uma construção coletiva
Vale destacar que a Tabela Periódica passou por diversas versões até chegar ao formato atual. A primeira versão eficaz foi criada por Dmitri Mendeleiev em 1869, que organizou os elementos por massa atômica e deixou espaços para elementos que ainda seriam descobertos.
Posteriormente, em 1913, Henry Moseley propôs a organização por número atômico, o que corrigiu imperfeições e tornou a Tabela mais precisa.
William Ramsay, por sua vez, foi responsável por descobrir os gases nobres, e Glenn Seaborg, na década de 1940, reconfigurou a Tabela ao adicionar os actinídeos abaixo dos lantanídeos.
Cabe ressaltar que, em 2019, os 150 anos da Tabela Periódica foram celebrados pela ONU e pela UNESCO com o Ano Internacional da Tabela Periódica dos Elementos Químicos.
Novidades recentes: elementos superpesados e homenagem a cientistas
Em 2016, a IUPAC oficializou a inclusão de novos elementos:
- Tennessine (Ts)
- Nihonium (Nh)
- Moscovium (Mc)
- Oganesson (Og)
Esses elementos, chamados de superpesados, têm um número muito elevado de prótons e são produzidos artificialmente em laboratório. Por isso, são instáveis e têm vida útil extremamente curta.
Desse jeito, a Tabela Periódica se mantém em constante atualização, refletindo os avanços científicos. É importante lembrar que o elemento 106 foi batizado de Seabórgio, em homenagem ao cientista Glenn Seaborg, que descobriu todos os elementos transurânicos (números 94 a 102).
Hidrogênio: um elemento à parte na Tabela
Embora apareça acima do Grupo 1 (Metais Alcalinos), o hidrogênio não pertence a essa família. Ele está ali por causa da sua configuração eletrônica, mas apresenta características muito distintas dos demais.
Portanto, sua posição é estratégica e simbólica, e não exatamente uma relação química direta com o grupo que o acompanha na tabela.
Curiosidades que tornam a Tabela ainda mais fascinante
- A IUPAC, órgão responsável pelas atualizações da Tabela, é uma ONG científica internacional.
- O fósforo foi o primeiro elemento isolado em laboratório, há mais de 350 anos, pelo alquimista alemão Henning Brand.
- O nome de diversos elementos homenageia cientistas, países ou regiões. Um exemplo é o Moscovium, em referência à cidade de Moscou.
Compreender a lógica da Tabela Periódica é muito mais do que decorar símbolos: é entender como a matéria se comporta, como os átomos se organizam e interagem.
Além disso, é uma habilidade essencial para interpretar questões do ENEM e vestibulares, onde o raciocínio químico muitas vezes é mais cobrado do que a simples memorização.
Sendo assim, dedicar tempo para entender a Tabela Periódica é investir diretamente na sua performance acadêmica. E agora que você conhece suas bases, história e estrutura, fica bem mais fácil encarar esse desafio de forma leve e eficiente.

