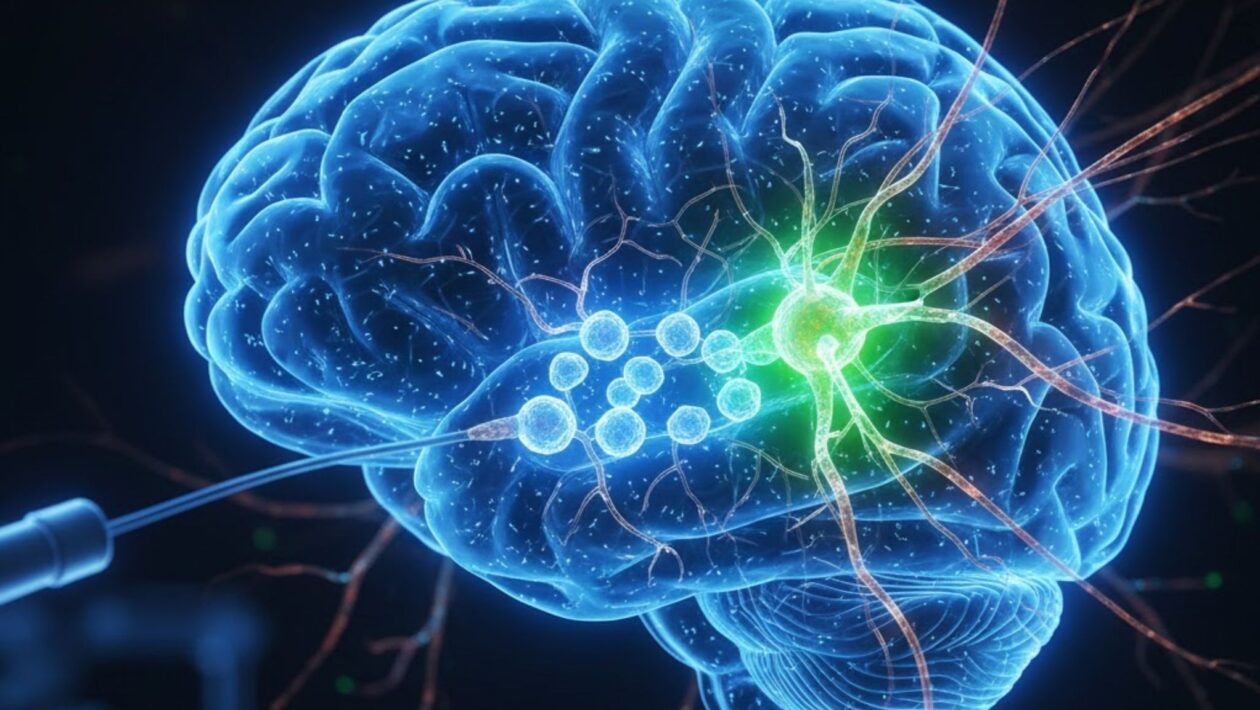
A busca por terapias capazes de ir além do controle dos sintomas da doença de Parkinson acaba de ganhar um novo capítulo. Um ensaio clínico em fase inicial está avaliando o implante de células-tronco produtoras de dopamina diretamente no cérebro de pacientes, com o objetivo de restaurar funções motoras comprometidas pela progressão da doença.
Atualmente, os tratamentos disponíveis reduzem tremores, rigidez e lentidão de movimentos. No entanto, nenhum deles consegue interromper a degeneração neuronal. Por isso, estratégias que visam recompor a base biológica do problema despertam grande interesse na comunidade científica.
Por que a dopamina é tão importante?
A dopamina é um neurotransmissor essencial para o controle motor, além de participar de processos ligados à memória, motivação e humor. Na doença de Parkinson, ocorre a morte progressiva dos neurônios dopaminérgicos localizados em regiões profundas do cérebro.
Como consequência, o organismo perde a capacidade de regular adequadamente os movimentos. Esse desequilíbrio resulta nos sintomas clássicos, que incluem:
• Tremores em repouso
• Rigidez muscular
• Lentidão dos movimentos
• Alterações no equilíbrio
Diante desse cenário, restaurar a produção de dopamina tornou-se um dos principais alvos terapêuticos.
Células adultas reprogramadas para produzir dopamina
O estudo conduzido pela Keck Medicine da USC utiliza células-tronco pluripotentes induzidas, conhecidas como iPSCs. Essas células são geradas a partir de tecidos adultos, como pele ou sangue, que passam por um processo de reprogramação genética até adquirirem capacidade de se transformar em diferentes tipos celulares.
Posteriormente, elas são direcionadas para se diferenciar em neurônios dopaminérgicos. A proposta é simples em teoria, mas complexa na prática: substituir células perdidas por novas células capazes de produzir dopamina de forma contínua.
Diferentemente das células-tronco embrionárias, as iPSCs reduzem questões éticas e ampliam as possibilidades de personalização terapêutica. Além disso, apresentam potencial para integração funcional no tecido cerebral.
Como funciona o procedimento
O implante é realizado por meio de uma pequena abertura no crânio. Com auxílio de ressonância magnética, os médicos posicionam as células nos gânglios da base, área crucial para a coordenação motora.
Após a cirurgia, os participantes são monitorados por um período de 12 a 15 meses. O acompanhamento inclui avaliação de:
• Evolução dos sintomas motores
• Possíveis efeitos adversos
• Risco de discinesias
• Sinais de infecção ou rejeição
O plano de seguimento se estende por até cinco anos, permitindo observar segurança e eficácia em longo prazo.
Prioridade regulatória nos Estados Unidos
O ensaio clínico multicêntrico envolve 12 pacientes com Parkinson moderado a moderadamente grave. A terapia experimental, chamada RNDP-001, foi desenvolvida pela empresa de biotecnologia Kenai Therapeutics.
A Food and Drug Administration dos Estados Unidos concedeu ao estudo a designação de via rápida, o que pode acelerar etapas regulatórias, caso os resultados demonstrem segurança e benefício clínico.
O que essa abordagem pode significar para o futuro
Se os resultados forem positivos, a terapia com células-tronco poderá representar uma mudança de paradigma. Em vez de apenas compensar a falta de dopamina com medicamentos, a estratégia tenta restaurar a capacidade natural do cérebro de produzi-la.
Ainda é cedo para falar em cura. Contudo, a possibilidade de retardar a progressão da doença e recuperar parte da função motora sinaliza um avanço promissor. À medida que a medicina regenerativa evolui, intervenções baseadas em terapia celular tendem a ocupar espaço crescente no tratamento de doenças neurodegenerativas.
O Parkinson continua sendo um desafio global. Porém, iniciativas como essa reforçam que a ciência está cada vez mais próxima de transformar esperança em realidade clínica.